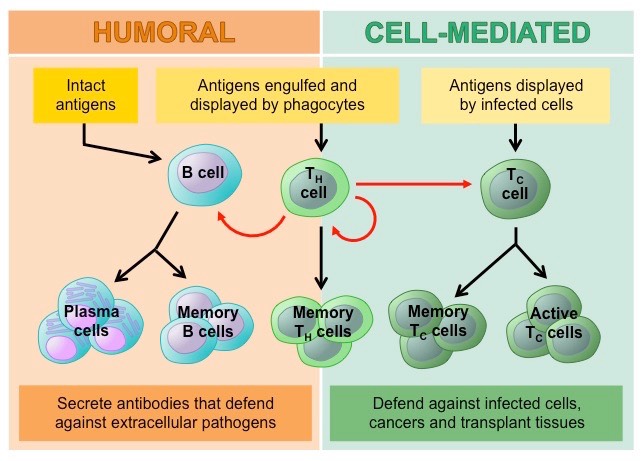
B hücrlerine dayalı humoral (antikor temelli) bağışıklık ve T hücrlerine dayalı hücre-aracılı bağışıklık, insan vücudunun kendisini bakteri, virüs ve toksinler gibi zararlı maddelere karşı hedefli bir şekilde savunmasını sağlayan iki tür uyarlanabilir (adaptif veya kazanılmış) bağışıklık tepkisidir. İmmün yanıtın bu kolları arasında bir miktar örtüşme olsa da, her ikisi de lenfoid hücrelerin işlevlerine dayanır ve bazı önemli farklılıklar da vardır.
Daha önce aynı enfeksiyona maruz kalmış birinden alınan antikorlarla birlikte uygulandığında, spesifik bir enfeksiyona veya hastalığa karşı humoral bağışıklık kazanılabilir. Bununla birlikte, antikor-aracılı bağışıklık, hücre aracılı bağışıklıktan farklı olan bir dizi moleküler bileşen ve işlem içerir. Bu yazıda, farklı immün süreçleri, amaçları ve önemli hücre tiplerini tartışarak humoral immünite ve hücre-aracılı immüniteyi tanımlıyoruz.

Humoral bağışıklık nedir?
Humoral bağışıklık , vücutta yabancı materyal (antijenler) tespit edildiğinde ortaya çıkan, antikor-aracılı bir tepkidir. Bu yabancı ajanlar tipik olarak bakteri ve virüsler gibi sırası ile hücre dışı ve hücre içi istilacılar olabilir. Bu mekanizma, esas olarak, spesifik bir antijenin saptanmasından sonra antikorlar üreten bir tür bağışıklık hücresi olan B hücresi lenfositleri tarafından yönlendirilir. (bkz. Doğuştan ve Uyarlanabilir Bağışıklık)
Naif B hücreleri, lenfatik sistemde vücutta dolaşan lenfositlerdir. Bu lenfositler, insan vücudundaki bulaşıcı ajanların saptanması için gerekli olan çeşitli antijene özgü molekülleri ifade ederler. Naif B hücreleri, lenfatik sistemde bir yabancı (antijen) ile karşılaştıklarında, hafıza B hücrelerinin ve efektör B hücrelerinin oluşumuna yol açan bir farklılaşma sürecinden girerler.

Bu farklılaşma sırasında hafıza B hücreleri ve efektör B hücreleri, atasal B hücreleri ile aynı antijene özgü molekülleri üretir. T hücresi lenfositlerinin yardımıyla ve mikrobiyal ilişkili antijenleri tanıyan MHC sınıf II reseptörleri tarafından aktive edilmiş “hafıza B hücreleri” yüzeylerinde bu antijene özgü molekülleri ifade ederken, “efektör B hücreleri” bu molekülleri ilgi antijene bağlanmak için kana salgılar.


Antikor nedir?
Antikorlar, yaklaşık 10 nanometre büyüklüğünde büyük proteinlerdir. Bu moleküller, patojenik bakteriler, mantarlar ve virüsler gibi zararlı maddeleri tanımak ve etkisiz hale getirmek için B hücreleri tarafından üretilir. Bu Y şeklindeki proteinler, hedef antijenlerine spesifik olarak bağlanan antijen bağlama domeynleri (bölge) içerir.

Antikorlar, hedef antijenlere etkili bir şekilde bağlandıktan sonra, ya hedef antijenlerini doğrudan bloke ederek nötralize ederler ya da antijenlerin uzaklaştırılmasını veya yok edilmesini teşvik eden diğer bağışıklık hücrelerinin veya moleküllerinin görevlendirilmesini indükleyebilirler. Memelilerde, bu tür antikorlar, genellikle “izotipler” olarak bilinen çeşitli formlarda gelir.
Antikorlar nasıl üretilir?
Her B hücresi, özel bir antijene özgü bağlanma bölgelerine sahip kendi antikor setini üretir. Başlangıçta, naif B hücreleri, kendi yüzeyine bağlı kalan antikorlar üretir, böylece bunların antijen bağlama bölgeleri potansiyel patojenleri, toksinleri ve yabancı maddeleri tespit edebilir. Bir antikorun bu yüzeye bağlı formu, bir “immünoglobulin” olarak bilinir.
Antijen bağlama domeyni ile eşleşen bir antijen, naif veya hafıza B hücresine bağlandığında, antijene spesifik daha fazla antikor üretmek ve salgılamak için B hücresini aktive eder. Bir B hücresi tamamen olgunlaştığında, “plazma hücresi” olarak bilinir ve yaşam döngüsünün geri kalanında antijene özgü antikorlar üretmeye ve salgılamaya devam edecektir.
Antikorlar patojenlerle savaşmak için ne yapar?
Antikorlar kan dolaşımına girdikten sonra (humoral), serbest yüzen bu proteinler, doğrudan ve dolaylı bağışıklık fonksiyonlarına sahip savunma molekülleri olarak işlev görmeye hazırdır. Bu işlevler şunları içerir:
- bulaşıcı ajanların nötralizasyonu (bloke etme veya antikor-bağımlı hücresel sitotoksisite)
- kompleman sistemin aktivasyonu (hücre-bağımlı sitotoksisite)
- yok edilecek yabancı maddelerin bağlanması (opsonizasyon ve fagositoz)
Antikorlar, öncelikle bağlanma ve birikim mekanizmaları yoluyla antijenleri nötralize eder. Örneğin, antijenle eşleşen viral partiküller üzerinde nötralize edici antikorların toplanması, bu virüsün diğer hücreleri enfekte etme yeteneğini bloke edecektir.
Antikorlar ayrıca, kompleman kaskadının aktivasyonu veya efektör hücreler ile etkileşim ve sitokinlerin salınması yoluyla enfekte veya antijen sunan hücrelerin lizisine (erime) veya öldürülmesine yol açan işlemlere de katılabilir. Kompleman sistemi, antikorların ve lenfositlerin vücudu patojenlerden ve enfekte olmuş hücrelerden temizleme yeteneğini artıran doğal bağışıklığın bir parçasıdır. Son olarak, patojenleri veya enfekte hücreleri kaplayan antikorlar, fagositoz sırasında makrofajları çekebilir (opsonizasyon) ve onlar tarafından yutulabilirler .
Hümoral bağışıklık, lenfositlerin antikor aracılı işlevler yoluyla enfeksiyona karşı koruma sağlamasına bağlıdır, ancak kemik iliği lenfositlerini içeren tek adaptif bağışıklık biçimi değildir.
Humoral ve hücre aracılı bağışıklık
| Humoral | Hücre Aracılı | |
| Tür | Antikor-aracılı yanıt | T-hücre aracılı yanıt |
| Faaliyet Yeri | Hücre dışı sıvılar | Antijen sunan dokunun yeri |
| İlgili Ana Hücre Türleri | B hücreleri | T hücreleri |
| Başlangıç Hızı | Tespit üzerine hızlı yanıt | Yavaş yanıt |
| Antijen Türü | Hücre dışı patojenler | Hücre içi patojenler, kanser hücreleri |
| Kaldırma Yöntemi | Antikor-aracılı yıkım veya nötralizasyon | Hücre lizisi ve programlanmış ölüm (apoptoz) |
| İlgili MHC Proteinleri | MHC sınıf II proteinleri | MHC sınıf I proteinleri |
Hücre-aracılı bağışıklık nedir?
Hümoral bağışıklığın aksine, hücre-aracılı bağışıklık adaptif immün fonksiyonları için antikorlara bağlı değildir. Hücre aracılı bağışıklık, öncelikle olgun T hücreleri, makrofajlar ve bir antijene yanıt olarak sitokinlerin salımı ile yönlendirilir. Hücre aracılı bağışıklığa dahil olan T hücreleri , hücre içi hedef antijenleri tanımak için membrana bağlı MHC sınıf I proteinleri içeren antijen sunan hücrelere dayanır. MHC proteinleri ve yabancı antijenler arasındaki bağlanma spesifitesi, naif T hücrelerinin yardımcı T hücrlerine veya öldürücü T hücrelerine olgunlaşması ve farklılaşması için gereklidir.
Hücre-aracılı bağışıklık tipik olarak, hücrelerin bir virüs, bakteri veya mantar (hücre içi istilacılar) tarafından enfekte olduğu vücut bölgelerinde devreye girer. MHC sınıf I proteinlerinin yardımıyla, T hücreleri kanserli hücreleri de tanıyabilir.
Hücre aracılı bağışıklıkta hangi lenfositler yer alır?
Hücre aracılı bağışıklığa dahil olan ana lenfosit tipleri arasında yardımcı (helper) T hücreleri, öldürücü (killer) T hücreleri ve makrofajlar bulunur. Bir “yardımcı” T hücresi vücutta antijen sunan bir hücre bulduğunda, sitokin adı verilen bir dizi sinyal proteinini salgılar . Bu sitokinler, antijen sunan hücreleri yok etmek için “öldürücü” T hücrelerini ve makrofajları ilgili bölgeye hareket etmek üzere aktive eder.
Naif T hücrelerinde bulunan T hücre reseptörleri (TCR’ler), majör doku-uyumluluk kompleksi (MHC) sınıf I proteinlerine bağlı spesifik antijenleri tanıdığında, olgunlaşır ve temel bağışıklık fonksiyonlarını yerine getiren özel bir T hücre tipi alt kümesine dönüşürler.
Genellikle sitotoksik T lenfositler (CTL’ler) olarak adlandırılan CD8+ T hücreleri, yüzeylerinde CD8 ifade eden bir alt popülasyona aittir. CD8, CD8+ T hücrelerinin MHC sınıf I proteinleri tarafından sunulan peptitleri tanımasını sağlayan dimerik (ikili) bir yardımcı reseptördür.

MHC sınıf I ile MHC sınıf II arasındaki fark nedir?
Ana doku-uyumluluk kompleksi (MHC), bağışıklık sisteminin yabancı maddeleri tanınması bir dizi gen tarafından kodlanan glikoprotein moleküllerini içerir. MHC moleküllerinin iki ana sınıfı vardır: MHC ı ve MHC II. Aralarında önemli farklar bulunur.MHC sınıf I molekülleri, bir organizmadaki tüm çekirdekli (nukleuslu) hücrelerin yüzeyinde ifade edilir. “Kendi” hücre içi antijenlerin sunumunda önemli bir role sahiptirler. Hücreler, virüsler gibi hücre içi patojenler tarafından enfekte olduğunda, MHC sınıf I proteinleri, hücrenin yok edilmesi gerektiğini bağışıklık sisteminin diğer bileşenlerine belirtmek için hücre yüzeyinde hedef patojenin protein parçalarını bağlar ve görüntüler.
MHC sınıf II molekülleri, yalnızca antijen sunan hücreler olarak adlandırılan bağışıklık hücrelerinin bir alt kümesi tarafından ifade edilir. MHC sınıf II tanıma, CD4+ yardımcı T hücresi gibi lenfositlere sinyal gönderme yoluyla adaptif bağışıklık tepkisinin başlatılması için esastır.
CD4+ lenfositleri, doğrudan ve dolaylı mekanizmalar yoluyla diğer bağışıklık hücresi aktivitesine aracılık eden bir “yardımcı” T hücreleri grubudur. Naif CD4+ T hücreleri, hedef antijenlerinin bağlı olduğu MHC sınıf II proteinlerini eksprese eden APC’ler tarafından uyarılana kadar timusta kalır. Bu protein kompleksinin başarılı bağlanması, CD4+ T hücrelerini yardımcı hücre tipine farklılaşmalarına başlamak için aktive eder. Aktive edilmiş CD4+ T hücreleri, CD8+ T hücreleri gibi sitotoksik işlevleri yerine getirmese de , sitokinlerin salgılanması yoluyla hümoral veya hücre aracılı bağışıklık tepkilerine aracılık edebilen yardımcı T hücre tiplerine olgunlaşırlar.
| Karşılaştırmak | CD8+ T hücreleri | CD4+ T hücreleri |
| Tip | Sitotoksik veya “öldürücü” hücreler | “Yardımcı” hücreler |
| Tuş işlev(ler)i | Enfekte veya kötü huylu hücreleri yok etmek | Bağışıklık hücre aktivitesine aracılık etmek |
| TCR-MHC bağlama kompleksi | CD8 + MHC sınıf I | CD4 + MHC sınıf II |
| Alt tür sayısı | Beş | Altı |
Timusta, naif bir CD8+ T hücresi ile antijen sunan bir hücre (APC) arasındaki başarılı bağlanma, olgunlaşmamış T hücresini sitotoksik işlevselliğe sahip aktifleştirilmiş bir CD8+ T hücresi haline gelmesi için uyarır. Hücre içi patojenlerin ve tümör hücrelerinin öldürülmesi gibi sitotoksik (hücre oldürücü) yeteneklere sahip olan CTL’ler, hücre aracılı adaptif bağışıklıkta yer alan bir grup özel lenfosite aittir. CTL’ler işlevsel bir bağışıklık sistemi için gerekli olmakla birlikte, CTL’lerin düzensizliği, diyabet veya artrit gibi organa özgü otoimmün hastalıkların patogenezine de yol açabilirler.

CD8+ T hücrelerinin apoptozu (programlı hücre ölümünü) başlatmasının bir yolu, iki tip sitotoksik protein olan perforin ve granzimlerin salgılanmasıdır. Perforinler, hedeflenen hücrelerin hücre zarında gözenekler oluşturan sitolitik (hücre eritici) proteinlerdir. CTL’ler, sitozol içinde apoptoz sürecini sürdüren bir serin proteaz sınıfı olan granzimlerin salınımını yönlendirmek için bu gözenekleri kullanır. Bu proteazlar, normal hücre bakımında yer alan viral ve hücresel proteinleri parçalayarak hedef hücreleri bozar. Apoptoz geçiren hedef hücreler daha sonra yakındaki fagositler tarafından temizlenir (yutulur ve sindirilir).
CTL’ler ayrıca Fas-Fas ligand etkileşimleri yoluyla apoptozu indükleyebilir. Fas ligandı (FasL), hedeflenen hücrelerdeki Fas reseptörüne bağlandığında, bir dizi sinyal molekülü, kaspaz proteazlarının aktivasyonu yoluyla apoptozu başlatır. Bu kaspazlar, apoptozun sonraki aşamaları boyunca proteolizin (protein parçalanmasını) büyük kısmını gerçekleştirir. Yönlendirilmiş apoptoza ek olarak, CD8+ T hücreleri, TNF- α gibi sitokin faktörlerinin salınımı yoluyla dolaylı olarak hedef hücreleri öldürebilir. Örneğin, tip 1 CD8+ T hücreleri (Tc1), viral replikasyonu inhibe edebilen ve spesifik antijen sunumunu güçlendirebilen bir sitokin olan IFN-gama’yı serbest bırakabilir. Birincil tepkilerinin sonunda, aktive edilmiş CD8+ T hücreleri tipik olarak apoptoz yoluyla ölür.
https://www.technologynetworks.com/immunology/articles/humoral-vs-cell-mediated-immunity-344829